赛箔合作|《Chem. Eng. J.》生物3D打印可传代GBM原代肿微组织,多靶点CAR-T精准评估

先导小贴士
近日,赛箔生物联合益诺思股份、中国药科大学、华山医院、上海中医药大学、先博生物等研究团队开展“产学研医”联合攻关,基于赛箔的生物材料研发平台和生物3D打印组织制造平台,成功构建可传代的生物3D打印患者来源胶质母细胞瘤微组织,实现对多靶点CAR-T的精准药效评价。
研究结果近日发表于 《Chemical Engineering Journal》(材料科学1区TOP,IF=13.2),题为“《Patient-derived 3D bioprinted glioblastoma models with defined physicochemical ECM properties for long-term maintenance and CAR-T therapy evaluation》”。
中枢神经系统肿瘤包含多种病理实体,包括原发性肿瘤和脑转移瘤。胶质母细胞瘤(GBM)是成人中最常见的原发性恶性脑肿瘤,因其侵袭性和浸润性特征,其预后始终不佳。尽管进行了大量的临床试验,但过去十多年来的标准治疗方案,仅能略微延长患者的中位生存期。证据表明,肿瘤的异质性和复杂的肿瘤微环境(TME),对GBM的治疗反应具有关键影响。值得注意的是,在临床前模型中显示出疗效的化合物,在临床试验中往往未能给患者带来显著的生存获益,这表明当前模型系统的预测能力存在不足。因此,亟需建立能够准确再现肿瘤TME且具有生理相关性的临床前模型。

研究亮点
1. 开发了一种3D生物打印平台,该平台能够支持患者来源的GBM 3D模型连续培养6周或进行5次连续传代。
2. 优化了用于GBM 3D模型的特定生物材料配方,以实现高细胞存活率和稳定的结构形成。
3. 建立了标准化的GBM 3D模型,保留了原始肿瘤组织的组织学特征、细胞异质性与体细胞突变。
4. 与CAR-T细胞的共培养实验揭示了抗原依赖性的细胞溶解作用和预测性的免疫治疗反应。

研究内容
模拟GBM细胞外基质的生物墨水筛选和打印参数优化
为了模拟GBM的天然细胞外基质成分(透明质酸含量较高),选择HAMA和GelMA制备生物墨水。通过一系列实验系统评估不同浓度组合HAMA和GelMA生物墨水的力学性能、黏度和形貌特征,确定符合GBM组织刚度范围和适宜细胞生长的最佳浓度组合为0.5% HAMA,4% GelMA,0.1%LAP。通过优化光固化3D生物打印过程中光照强度和曝光时间,确定最佳的打印条件。
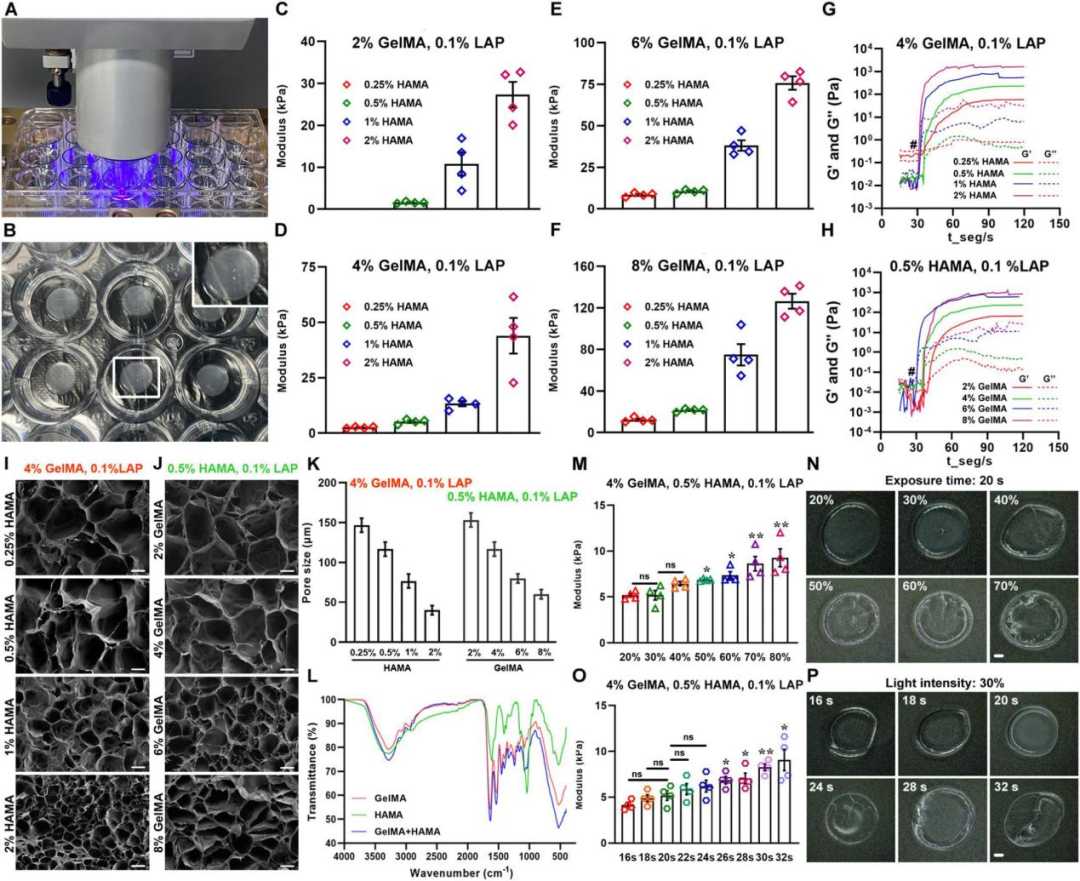
患者来源的GBM 3D模型的建立及长期培养
将GBM患者手术组织标本中分离出的原代细胞封装在4% GelMA,0.5% HAMA的生物墨水中,使用基于数字光处理(DLP)3D生物打印技术构建GBM体外模型。原代GBM细胞在水凝胶中表现出较强的的生长活性。在培养过程中,细胞球体直径最高达到150 μm。同时,本研究通过迭代生物打印过程实现了原代GBM细胞的传代培养,能够稳定传代达到5代以上。细胞在冻存、复苏之后仍保持高活性,这为肿瘤精准治疗和基础生物学研究提供了丰富的材料来源。
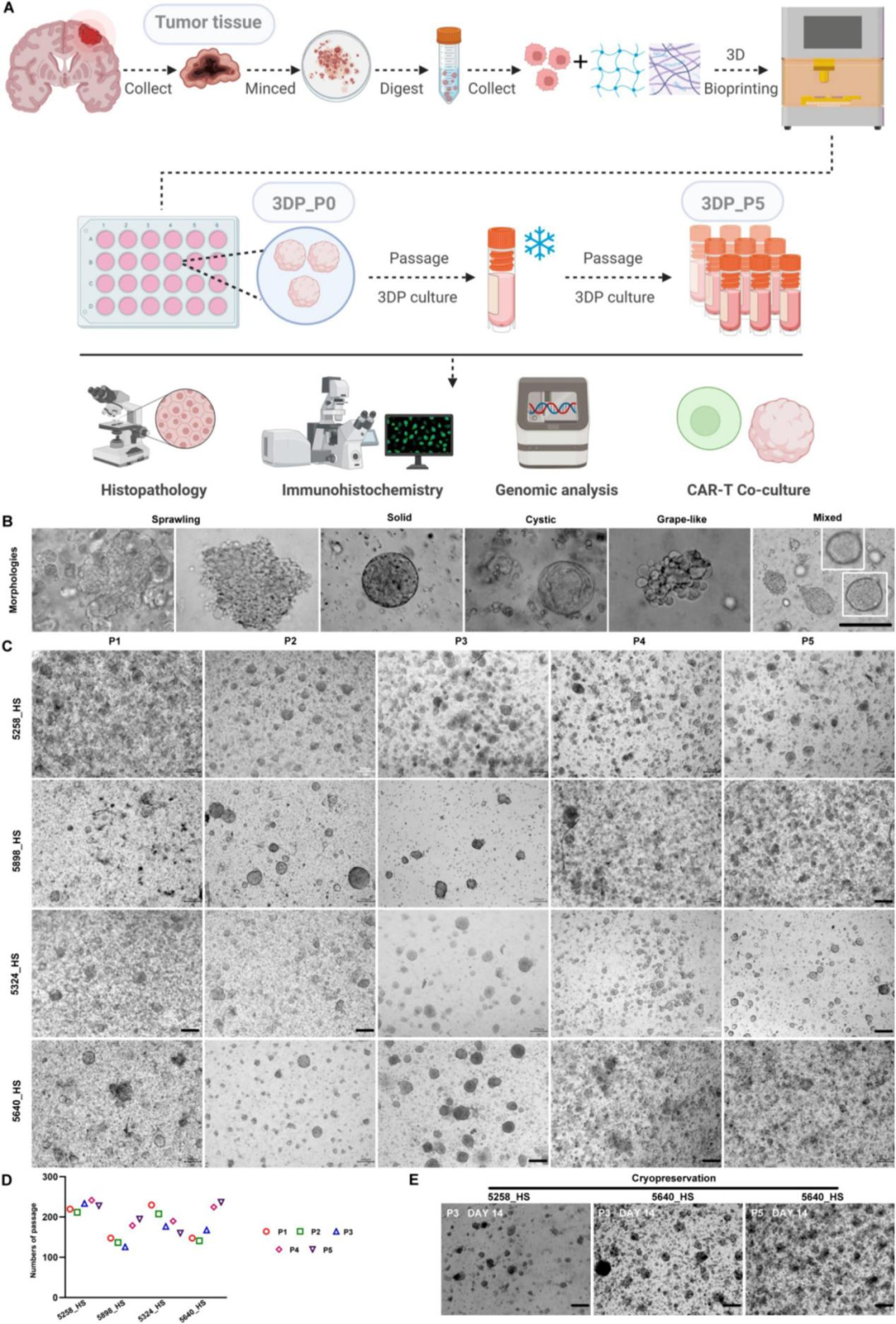
GBM 3D模型重现了原始肿瘤的组织病理学和细胞多样性特征
研究通过H&E染色和免疫荧光染色标记一系列标志物,包括GFAP、MAP2、DCX、NESTIN、SOX2和OLIG2,证实GBM 3D模型(P0)及其传代打印样本(P5)均保留了原始肿瘤的组织病理学特征和细胞多样性。同时,巨噬细胞/小胶质细胞标CD11b和Iba1也所保留。

GBM 3D模型在长期扩增过程中保持了基因组和表观基因组的完整性
将原始肿瘤组织及其对应的GBM 3D模型(P0)、连续传代模型(P5)进行全外显子测序、STR鉴定和DNA甲基化芯片检测分析。研究结果显示,原始肿瘤中存在的大多数体细胞变异在P0和P5模型中能被检测到。拷贝数变异(CNVs)在相应的P0和P5模型中也被准确地重现。同时,在传代过程中P5和P0的甲基化β值高度一致。结果表明,GBM 3D模型在长期扩增过程中保持了基因组和表观基因组的一致性和稳定性。
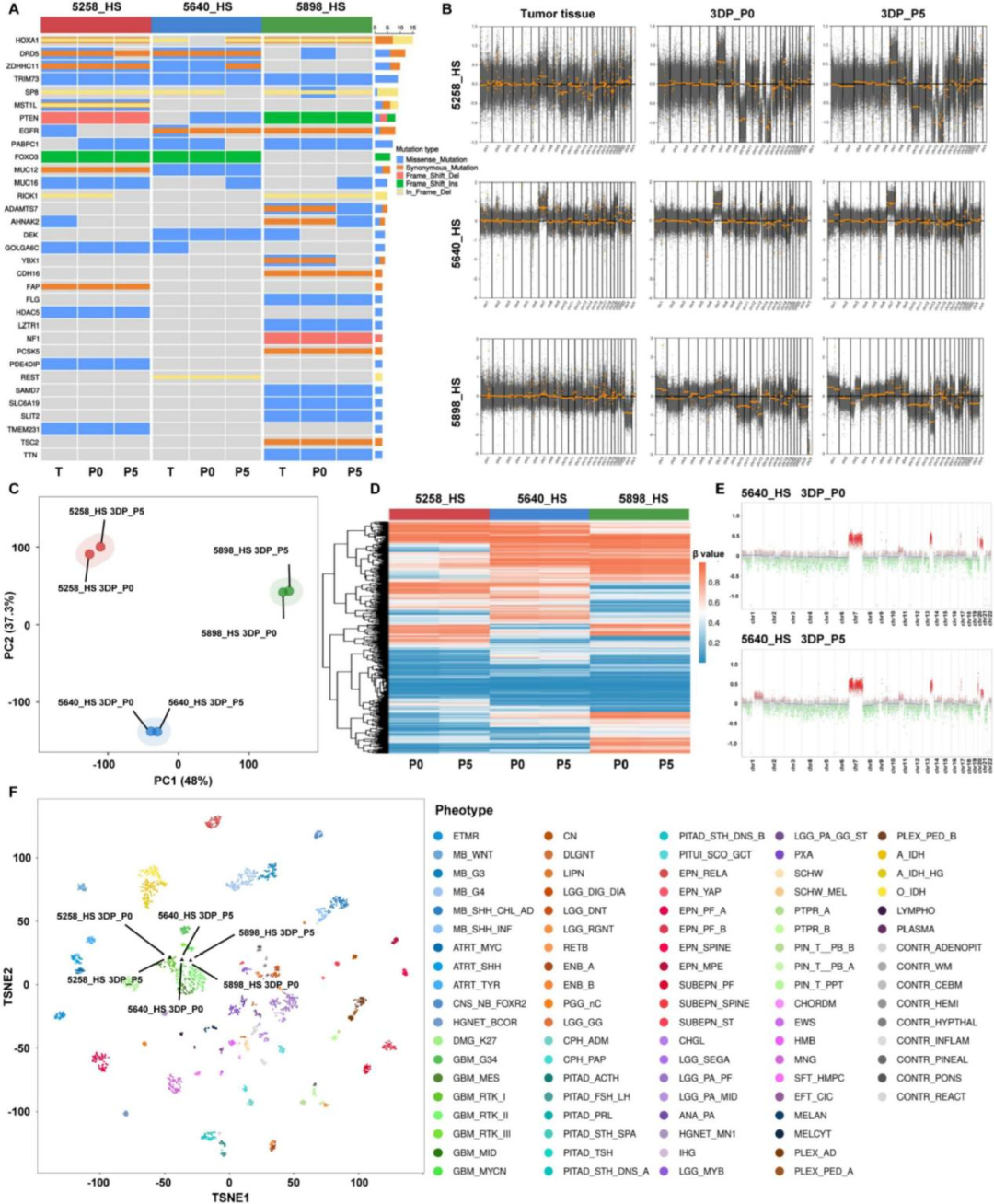
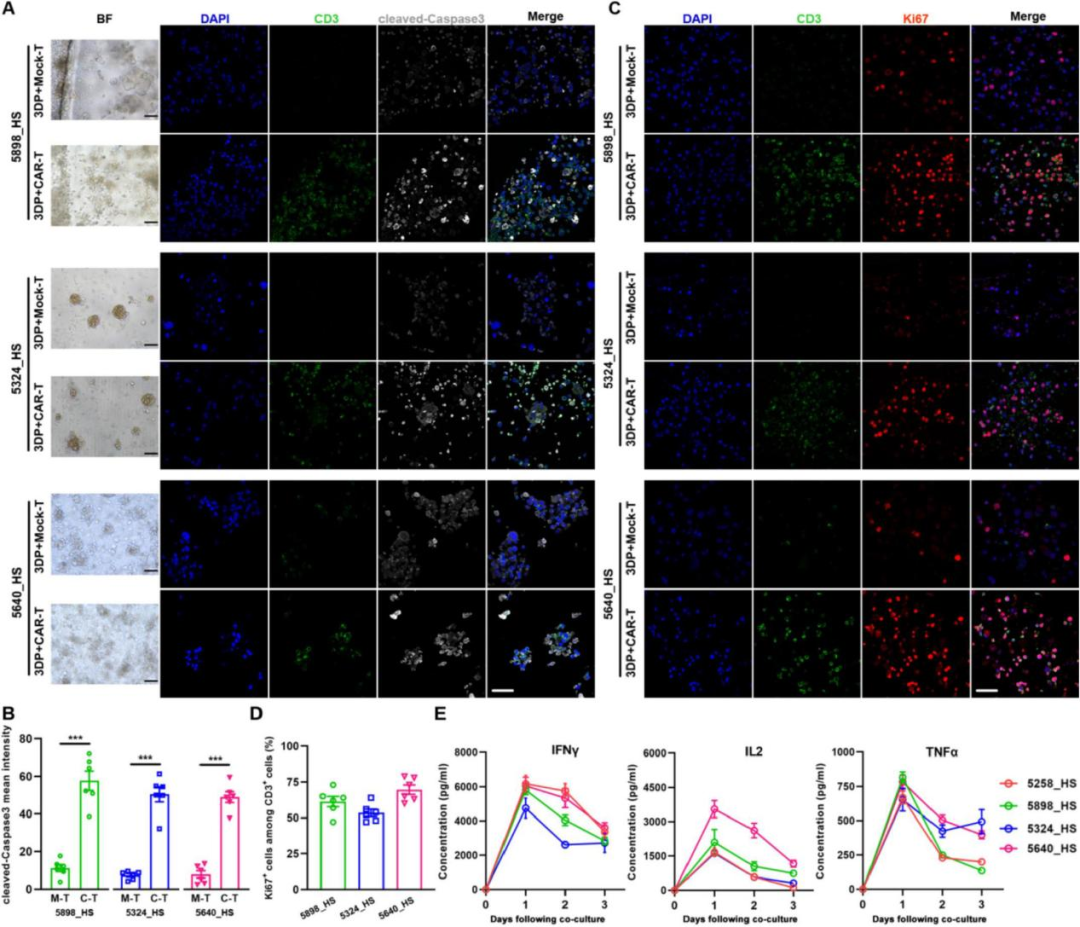
GBM 3D模型可用于评估CAR-T细胞免疫疗法的效果
将GBM 3D模型与特异性表达GBM靶抗原的CAR-T细胞共培养,检测T细胞增殖、肿瘤细胞死亡、EGFR/EGFRvIII抗原丢失以及细胞因子释放。与Mock-T细胞相比,在CAR-T细胞处理的GBM 3D模型中,表达CD3的T细胞均为Ki67+,表明有大量的T细胞增殖。同时,表达EGFR +和EGFRvⅢ+ +的肿瘤细胞Caspase3信号显著增强,表明CAR-T细胞对肿瘤细胞的靶向杀伤作用。ELISA检测到细胞因子IFNγ、IL2和TNFα的释放显著升高。其中,T细胞的激活强度与肿瘤细胞靶抗原的表达呈正相关。低表达EGFR的模型(5258和5898),其TNFα的释放水平也较低;而高表达EGFR的模型(5324和5640)在共培养中TNFα的含量更高。结果表明,GBM 3D模型在快速评估抗原特异性CAR-T细胞治疗反应中的应用价值。

总结
GBM 3D模型保留了原始肿瘤的关键组织学特征、肿瘤间和肿瘤内的异质性、基因突变模式以及微环境成分,为临床研究建立了一个高度精确的平台。重要的是,该研究能够在术后2-3周内成功生成患者特异性的GBM 3D模型。这种快速的时间框架有助于实时进行相关的治疗测试,为针对患者特异性治疗反应提供前瞻性见解。
关于赛箔生物
赛箔(上海)智能科技有限公司是一家专注于生物智造技术和组织工程产品研发的高新技术企业。围绕生物3D打印、组织工程与再生医学方向,开展体外人源模型和临床可植入组织产品的研发与转化。公司自主研发光固化生物3D打印机和高通量3D组织制备仪器,建立了器官成分数据库并相应开发适配不同健康和疾病组织的专用生物材料、培养试剂盒,形成了覆盖设备、材料、模型与应用服务的一体化技术体系。
在应用端,公司创立了3D打印肿瘤微组织(PDT)体外模型体系,性能优于传统类器官,已覆盖十九个癌种,包括高发肿瘤、难治肿瘤、妇科肿瘤和儿童肿瘤,细胞培养存活率超过90%。基于1000+患者样本研究,该体系已用于临床药敏检测、服务多家biotech与上市药企开展创新药评价。与上市CRO企业建立战略合作关系,共同提供围绕NAMs体外模型相关服务。
在再生医学领域,持续布局皮肤与眼科方向,采用自主研发的生物3D打印技术开展组织构建与产品开发,已在全层皮肤、毛囊和角膜方向形成阶段性进展。

肺癌
宫颈癌
结直肠癌
卵巢癌
脑胶质瘤
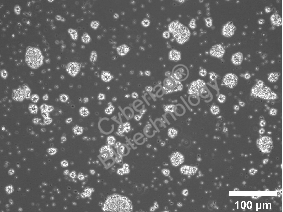
神经母细胞瘤
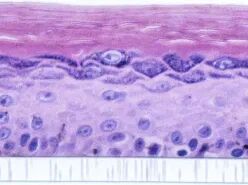
黑色素皮肤模型

全层皮肤模型
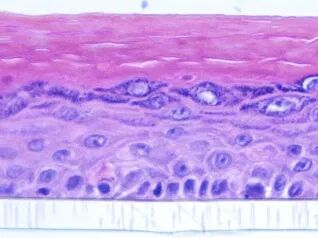
表皮模型


